
(사진출처 : 공학저널)
오늘은 금속의 성질과 금속의 연소에 대해 알아보도록 하겠습니다.
(사진출처 : 머릿속의 바람)
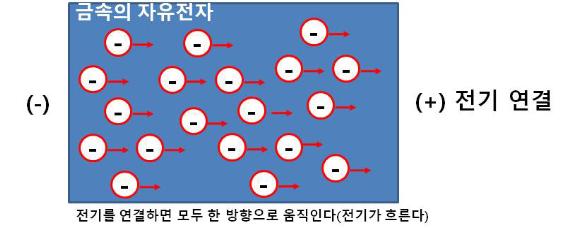
먼저 금속의 성질입니다. 금속은 원자에 소속되어 있지 않은 자유 전자라는 것이 있습니다. 이 자유 전자에 전기를 연결하면 모든 자유 전자가 한 방향으로 움직이면서 전기가 흐릅니다. 또한 열도 잘 전달하는데, 이를 열, 전기 전도성이라고 부릅니다. 또 잡아당기면 늘어나는 연성과 두드리면 얇게 펴지는 전성이 있습니다. 합쳐서 연전성이라고 부르기도 합니다. 그리고 금속은 빛을 대부분 반사해 빛이 나는데, 이 빛을 광택이라 부릅니다. 이 성질 중에서 하나라도 포함하지 않으면 그 물질은 금속이라 말할 수 없습니다. 단단하지만, 열, 전기 전도성과 광택이 없어 금속이 아닌 플라스틱이 그 예입니다. 가장 확인해보기 쉬운 성질은 광택이지만 산화되면 광택이 잘 나지 않기 때문에 알아보기 어렵습니다. 그래서 열, 전기 전도성을 가장 쉽게 확인해 볼 수 있습니다. 열은 한쪽을 데웠을 때 다른 쪽에서도 온도가 전달되는지를 보면 되고, 전기는 전기 회로를 끊어 놓고 그 자리에 금속을 놓았을 때 작동하는지를 보면 됩니다. 물론, 철인지를 알고 싶으면 자석으로 확인하는 것이 가장 쉽습니다.

(사진출처 : 시니어메일, 나트륨을 물에 넣었을 때의 모습)
그 다음으로 금속의 연소입니다. 금속이 무조건 불에 붙지 않는 것은 아닙니다. 철도 산소만 충분하면 타오릅니다. 나트륨은 물과 만나면 바로 산화하여 불이 붙습니다. 이는 나트륨이 산화되어 산화나트륨과 수소 가스가 만들어져서 수소가 공기중의 산소와 반응할 때 나는 열 때문에 불이 붙은 것입니다. 사건으로는 2012년 5월 22일 새벽에 일본의 금속 가공 공장에서 마그네슘에 불이 붙었던 경우가 있습니다. 물을 부으면 수소 가스가 발생하고 폭발하기 때문에 그대로 놔 두었고, 6일 뒤에 불이 꺼졌습니다. 금속도 불에 타니 항상 조심해야 합니다.
지금까지 공민호 기자였습니다. (2편도 곧 작성할 예정)
기사 평가화학기자단2021.08.19
시리즈 기사가 될 것 같은데, 이 기사를 기획하게 된 배경이 처음에 나왔으면 좋았을 것 같아요. 왜 금속성 물질을 다루려고 하는지를 독자들이 알고 읽는 것이 집중도와 주목도가 더 높기 때문이죠. 그리고 본문이 두 개인데, 이럴 경우 중간제목을 활용하는 것이 글 구성상 좋았을 것 같아요. 끝으로 일본 금속공장 화재 사건은 연도(201년?)를 확인하고 수정해 주기 바랍니다. [그다음으로] → [그 다음으로], [나두었고] → [놔 두었고]










