
(출처 : 네이버 블로그)
오늘은 나쁜 줄만 알았던 황사의 이로운 점에 대해 알아보겠습니다.
황사가 이로운 역할을 할 수 있는 데에는 황사의 성분이 중요합니다. 황사는 주성분인 황토에 포함된 석회나 산화 마그네슘 때문에 염기성을 띱니다. 여기서 염기성이란 단백질을 녹이고, 만지면 미끌거리는 등의 성질도 있지만 물에 녹아서 수산화 이온을 내며, PH→ pH(수소이온농도지수)가 7 이상인 물질인 염기의 성질을 염기성이라고 합니다. 그리고 이 염기성을 가진 물질을 염기성 물질이라고 합니다. 이 염기성인 황사와 산성인 빗물이 만나면 중성이 된다고 합니다.
(출처 : 네이버 블로그)
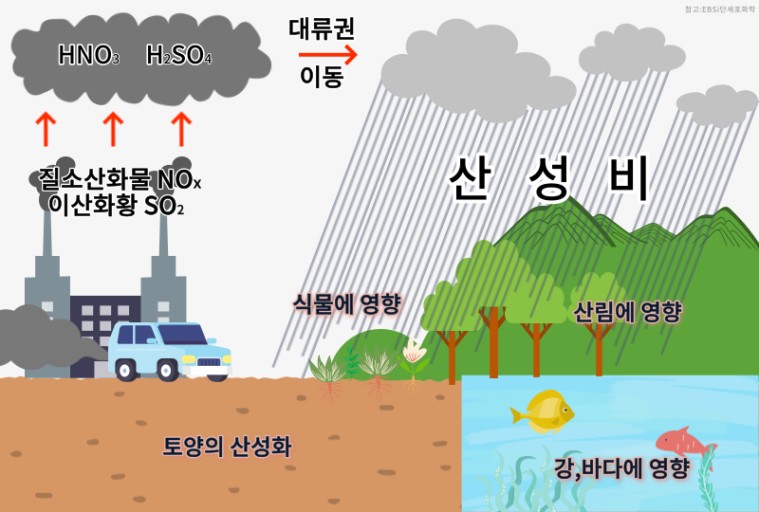
빗물이 산성이라는 사실에 산성비를 떠올리시는 분들도 있으시겠지만 비는 언제나 산성비가 아니여도 이산화 탄소 때문에 산성을 띱니다. 여기서 산성은 염기성과는 반대로 수소 이온을 내며, PH→ pH가 7 이하인 물질을 산이라고 하는데 이 산의 성질을 말합니다. (PH→ pH는 낮을수록 수소 이온이 많으며, PH→ pH가 1 작아질 때마다 수소 이온은 10배씩 많아집니다) 또한 금속과 반응하여 수소 기체를 발생시키고 단백질을 굳게 하는 성질도 있습니다. 만약에 공장에서 나온 질소산화물이나 이산화황이 섞이게 되면 빗물의 산성도는 훨씬 강해집니다.
그런데 황사와 빗물이 만났을 때 중성이 되는 이유는 황사 속의 수산화 이온과 빗물 속의 수소 이온이 만나 물로 변하고, 나머지 이온들이 결합해 염이라는 물질이 되는 중화 반응이 일어나기 때문입니다. 또한 황사는 햇빛을 분산시켜서 지구온난화를 늦춘다고도 합니다.
이렇게 황사가 꼭 나쁘기만 하다고 생각할 필요는 없습니다.
지금까지 공민호 기자였습니다.
기사 평가화학기자단2021.08.22
'황사가 좋은 영향도 미친다고?' 고개를 갸웃하며 기사를 열어 봤어요. 그런데 황사가 산성비를 중화시키는 역할을 한다니! 정말로 몰랐던 사실을 알게 됐어요. 그리고 이번 기사에서 pH가 여러 번 나오는데, 표기가 모두 잘못되어 있더라고요. PH가 아니라 pH로 쓰는 게 맞고요, 또 "PH(수소이온농도지수)가 7이하인 물질인 염기"라는 문장이 초반에 나오는데 염기는 7 이상인 물질을 말해요. 아래쪽에 산은 맞게 설명이 되어 있어서, 바로잡습니다. 과학 기사인 만큼 단위, 용어 등은 정확하게 표기해 주세요!








